主备:陶晓红
审核:化学备课组
【复习目标】
1.金属与合金的性质
2.金属与氧气、稀盐酸、稀硫酸等反应的不同
3.金属活动顺序及其应用
4.铁生锈的条件及其防护
5.有关杂质在化学方程式中的计算
【复习内容】
一、金属材料:
1.金属的物理共性:
、
、
、
。
2.地壳中含量最多的金属元素是
,第二多的是
;目前年产量最多的金属是
,居第二位是 ;人类最早使用的金属是
,其次是
。
3.合金:
。
4.生铁中含碳量
,钢中含碳量
;
5.合金与纯金属相比的优点:①
②
③
④
6.由于
与人体具有很好的
,因此可用来制造人造骨。
二、金属的化学性质
1.置换反应:
。形式:A+BC――
+
2.金属活动顺序
3.判断金属活动性强弱的依据
①
;②
;③
。
三、金属资源的利用和保护
1.地球上金属元素大多以
形式存在,少数以
形式存在。
2.矿石的主要成分:赤铁矿
,黄铁矿
,磁铁矿
,菱铁矿
,铝土矿
,孔雀石的主要成分是Cu2(OH)2CO3(碱式碳酸铜)
3.炼铁原料:
、
、
、
4.炼铁原理:
5.化学方程式中含杂质计算的关键是
6.铁生锈的条件
7.防止铁生锈的方法:
【巩固练习】
1.在109~107m范围内,对原子、分子进行操纵的纳米超分子技术往往能实现意想不到的变化。如纳米铜颗粒一遇到空气就会剧烈燃烧,甚至发生爆炸。下列说法正确的是(
)
A、纳米铜属于化合物
B、纳米铜颗粒比普通铜更容易与氧气发生反应
C、纳米铜颗粒比普通铜所含铜原子的种类不同
D、纳米铜无须密封保存
2.将适量的铁粉投入到盐酸中,下列现象不会出现的是
( )
A、溶液变成浅绿色
B、有无色气体产生 C、铁粉不断减少
D、有棕色沉淀产生
3.下列方程式书写正确的是
( )

A、2Fe+6HCl=2FeCl2+3H2↑
B、Fe+H2SO4=FeSO4+H2↑
C、2Fe+3CuSO4=Fe2(SO4)3+H2↑
D、4Fe+3O2======2Fe2O3
4.有X、Y、Z三种金属,将X、Y和Z分别浸入稀硫酸中,Z溶解,X、Y不溶解;将X、浸入Y的可溶性溶液中,在X表面有Y析出。则X、Y、Z的金属活动性按由强到弱的顺序是
A.Z、Y、X
B.Y、Z、X
C.Z、X、Y
D.Y、X、Z(
)
5.下列可用于验证铜、铁、锌三种金属的活动性强弱的一组药品是
( )
①Cu、Zn、FeSO4溶液
②Cu、Fe、ZnSO4溶液
③Zn、FeSO4溶液、CuSO4溶液
④Fe、CuSO4溶液、ZnSO4溶液
A、①④
B、①②
C、②③ D、③④
6、将铁放入下列溶液中,溶液质量会减少的是
( )
A、盐酸溶液
B、硫酸溶液 C、硫酸亚铁溶液
D、硫酸铜溶液

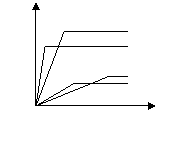 7.相同质量的铁、锌、镁、铝分别与足量的盐酸反应,产生氢气的质量与反应时间的关系如图所示,图中曲线①②③④对应的金属是
(
)
7.相同质量的铁、锌、镁、铝分别与足量的盐酸反应,产生氢气的质量与反应时间的关系如图所示,图中曲线①②③④对应的金属是
(
)
A、铝、镁、锌、铁
B、铁、锌、镁、铝
C、铝、镁、铁、锌
D、锌、镁、铁、铝
8.向溶解有硝酸银和硝酸铜的溶液中加入一定量的铁粉,充分反应后溶液中仍有金属固体,则滤液中一定存在的溶质是
( )
A、硝酸亚铁、硝酸银
B、硝酸亚铁、硝酸银 C、硫酸亚铁、硝酸银、硝酸银
D、硝酸亚铁
9.下列关于混合物分离与提纯的方法(括号中物质是杂质)中,不正确的是
( )
|
选项 |
混合物 |
分离与提纯的方法 |
|
A |
氯化钠(泥沙) |
混合物放入水中搅拌、溶解、过滤 |
|
B |
CO2(CO) |
混合物通入澄清石灰水后,再干燥剩余气体 |
|
C |
CaCl2(CaCO3) |
混合物溶解,滴加适量盐酸,蒸发、结晶 |
|
D |
Cu(Zn) |
混合物放入试管,滴加足量盐酸,过滤、洗涤、干燥 |

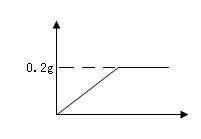 10.为了测定黄铜(铜、锌合金)的组成,某学习小组称取该样品10克,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的
10.为了测定黄铜(铜、锌合金)的组成,某学习小组称取该样品10克,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的
气体与所用硫酸溶液的质量关系如图所示。计算:
(1)样品中铜的质量分数;
(2)反应所消耗的硫酸的质量;


(3)反应后生成新物质的质量分别是多少?