【学习目标】
1.掌握一种溶液组成的表示方法――溶质的质量分数;
2.正确理解溶液的浓稀与溶液饱和程度的关系;
3.能进行溶质质量分数的简单计算
【学法指津】通过学生分组合作讨论、实验演示、老师指导来学习,培养学生动手能力、观察能力及分析解决问题的能力;
知识探究:
|
知识点 |
学生活动与探究 |
教师指导 |
|
一、
有色
溶液
浓稀
判断 |
【实验9-7】在三支试管中各加入20ml水,再分别加入约0.1g、0.5g、2g硫酸铜。观察溶液颜色是否一样?填下表
|
试管 |
溶液
颜色 |
溶剂
质量 |
溶质
质量 |
溶液
质量 |
溶质的
质量分数 |
|
1 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
3 |
|
|
|
|
|
【结论】同种溶质,溶液颜色
,浓度
;反之亦然。 |
温馨提示:
无水硫酸铜颜色是
五水硫酸铜颜色
(CuSO4+5H2O==CuSO4・5H2O
)
|
|
二、
溶质质量分数
|
1.定义或计算式:
【实验9-8】在90g水中加入10gNaCl和80g水中加入20gNaCl,观察现象,并计算溶液中溶质的质量分数。
|
溶质质量/g |
溶剂质量/g |
现象 |
溶液中溶质的质量分数 |
|
10 |
90 |
|
|
|
20 |
80 |
|
|
2.溶液中有不同溶质时,其溶质质量分数应分别计算。
如150克水中溶有20克蔗糖和30克食盐,则该溶液中溶质质量分数应为

3.同温同溶质,饱和溶液的浓度最大,溶质质量分数最大,计算式为
3.计算20℃时,氯化钠溶液、硝酸钾溶液中最大溶质质量分数分别为
、
。 |
思维点击:
溶质质量分数计算是以溶液质量为分母,不是溶剂质量
|
|
三、
溶质质量分数简单计算
|
1.溶质质量分数的基本计算

溶液中的基本要素:溶液质量、溶质质量、溶剂质量、溶质质量分数(a%)
同学们阅读课本P43页【例题一】,做课本46页【习题1】
2.溶液稀释的计算
关键①稀释前后
保持不变
②混合后溶液总质量等于
混合后溶质总质量等于
③计算时一定要将液体的体积转化为质量
阅读课本P44页【例题二】,做课本46页【习题2、3、4、5、6】 |
温馨提示:
1.溶液中的四要素知道任意2个,就可以求出数值
2.能灵活运用溶质质量分数计算公式的变形式。 |
经典例题剖析:
例1:100g98%浓硫酸与150g10%的稀硫酸混合后,所得溶液的溶质质量分数是多少?
分析:
溶液质量
溶质质量 溶质质量分数
混合前 ①
100g 98g 98%
②
150g 15g 10%
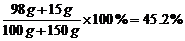 混合后
250g 113g ?
混合后
250g 113g ?
计算:溶质质量分数(a%)=
答:所得溶液的溶质质量分数为45.2%。
【课堂检测】
基础达标
1.对100克溶质质量分数为10%的某物质的溶液,分别进行如下操作:①加入10克水②加入10克同种溶质且完全溶解③加入溶质质量分数为10%的同种溶质的溶液④蒸发掉10克水且无晶体析出。操作后的四种溶液溶质质量分数分别是
。
2.t℃时,向硝酸钠饱和溶液中加入一定量的水后,下列有关该溶液的叙述正确的是(
)
A.仍为饱和溶液
B.溶质的质量变小
C.溶质的溶解度不变
D.溶质质量分数不变
3.t℃时,给某溶液(仅含一种溶质)恒温蒸发掉10克水,析出2克晶体,再恒温蒸发掉10克水,又析出3克晶体,则下列说法正确的是
( )
A.原溶液在t℃时一定是不饱和溶液
B.原溶液一定是稀溶液
C.最后剩余的溶液一定比原溶液稀
D.最后剩余溶液的溶质质量分数比原溶液的小
综合运用4.现有200克质量分数为10%的硝酸钠溶液,欲将其质量分数提高到15%,试计算:
①需要向此溶液中加入多少克硝酸钠?
②若采用向原溶液中加入质量分数为20%的硝酸钠溶液的方法,则需要这种溶液多少克?
5.一定温度下,将425
g含有A物质的溶液蒸发掉300
g水后,溶液恰好饱和;若另取 85
g原溶液,加入25 g A物质和
40 g水充分搅拌后,溶液也恰好饱和。求饱和溶液中溶质的质量分数是多少?
拓展延伸 无水硫酸铜颜色是
,五水硫酸铜颜色
,无水硫酸铜与五水硫酸铜可以相互转化,根据其颜色的变化,可以用无水硫酸铜来检验无水乙醇是否含有水。(
CuSO4 + 5H2O == CuSO4・5H2O
)
自我评价:(突出学习方法及本节课主要内)
签名: 年
月
日
同伴评价:(突出学习态度、过程表现与学习效果)
签名: 年
月
日
《课题3
溶质的质量分数(第2课时)》学案
主备:陶晓红
审核:化学备课组
【学习目标】
1.化学方程式中溶液的计算
2.初步掌握配制一定溶质质量分数的溶液的步骤
【学法指津】学生预习、练习、教师指导,培养学生严谨求实的态度,缜密地思维能力
知识回顾
欲将80g质量分数为20%的NaCl溶液稀释到质量分数为10%,需加多少克水?
知识探究
|
知识点 |
学生活动与探究 |
教师指导 |
|
一、
计算技巧
|
1、蒸发溶剂质量为原溶液质量的一半,若无溶质析出,则所得溶液中溶质质量分数为原溶液的两倍。
2、增加溶剂质量等于原溶液的质量,则所得溶液中溶质质量分数为原溶液的一半。
举例:(1)有200g溶质质量分数为5%的NaCl溶液,蒸发100g水后,所得溶液溶质质量分数为
(2)向50g6%的KNO3溶液中加入50g水,则所得溶液溶质质量分数为
。 |
|
|
二、
综合计算
三、
溶液的
配制 |
【例】实验室常用锌与稀硫酸反应来制取氢气。今取6.5g锌加入50g一定质量分数的硫酸溶液中,恰好完全反应,请计算:
①生成多少克氢气? ②硫酸溶液中溶质的质量分数
③反应后所得溶液中溶质的质量分数。
解:设①生成氢气的质量为x,②硫酸溶液中溶质的质量分数为a%,③生成ZnSO4的质量为y
Zn + H2SO4
=== ZnSO4 + H2↑
65 98 161 2
 6.5g
50g・a%
y x 6.5g
50g・a%
y x
①
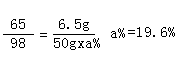
②

③
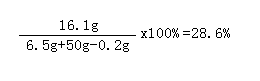
ZnSO4%=
答:①生成0.2克氢气;②硫酸溶液中溶质的质量分数为19.6%③反应后所得溶液中溶质的质量分数为28.6%。
阅读课本P47-48内容,归纳总结“配制溶质质量分数一定的溶液”
1、过程:①
、②
、③
、④
。
2、所需仪器:
3、操作不当对配制的溶液会造成的影响(偏大、偏小或无影响)
①称量不准确(多或少)
②左码右物
③天平未归零称量
④仰视量筒或俯视量筒
⑤量筒内的水未倒完
⑥烧杯中液体未完全转移到试剂瓶内
|
思维点击:
1、要认真审题,理解“充分反应”、“完全反应”、“恰好完全反应”的
区别;
2、反应后溶液质量计算,方法有两种:
①利用质量守恒定律反应后溶液的质量==参加反应物质的质量和―生成的气体质量―生成的沉淀质量,
②基本求法:溶液质量==溶质质量+溶剂质量
温馨提示:
你还能想出哪些不当操作?请写出并分析对配制溶液会造成的影响。 |
|
小结 |
|
经典例题剖析:
例:生铁和钢都是铁的合金。将一块质量为10.0g的铁合金放入锥形瓶中,再向锥形瓶中加入100g稀硫酸,恰好使铁合金中的铁完全反应(杂质不参加反应),测知生成氢气的体积为4.00L(ρH2=0.088g/L),问①该合金是生铁还是钢?②反应后所得溶液溶质的质量分数是多少?
分析:生铁的含碳量:2.0%~4.3%,钢的含碳量:0.03%~2%。应将氢气的体积换算成质量,由氢气的质量求出合金中铁的质量、生成的硫酸铁质量,进而求出合金中含碳量及溶液中溶质质量分数。
解:设①合金中铁的质量为x;②生成硫酸亚铁的质量为y
Fe + H2SO4
=== Fe SO4 + H2↑
56 152 2
x y 4.00L×0.088g/L=0.352g
①
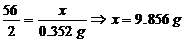

c%= ∴是钢
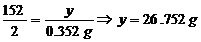
②

FeSO4%=
答:①该合金是钢;②反应后所得溶液溶质的质量分数是24.4%。
【课堂检测】
基础达标
1.现有80g质量分数为10%的硝酸钠溶液,试回答下列问题:
①上述硝酸钠溶液中含溶质的质量是
g,溶剂的质量是
g;
②若向上述溶液中加入20g水,则所得溶液中溶质质量分数是
;
③若向上述溶液中加入20g硝酸钠,则所得溶液中溶质质量分数是
;
④若使上述溶液中溶质质量分数变为20%,则应加入硝酸钠
g;
⑤若使上述溶液中溶质质量分数变为20%,则应蒸发水
g;
⑥若使上述溶液中溶质质量分数变为5%,则应加入
g水。
综合运用
2.课本P45页第8题(在下面写出过程)
拓展延伸
3.30℃时Ca(OH)2在水中的溶解度为0.16g/100g水。在此温度下,实验小组为制备饱和的澄清石灰水,称取5.6g生石灰,放入1000g水中,充分搅拌后冷却至30℃,过滤得到的澄清石灰水中溶质的质量
( )
A、等于5.6g
B、大于5.6g
C、等于1.6g D、小于1.6g
自我评价:(突出学习方法及本节课主要内)
签名: 年
月
日
同伴评价:(突出学习态度、过程表现与学习效果)
签名: 年
月
日