【学习目标】
1.
认识二氧化碳的主要物理性质和化学性质;
2
通过观察和描述有关二氧化碳的实验现象,从中归纳出二氧化碳的某些性质;
【学法指津】科学探究、实验――讨论――归纳,让学生主动参与教学活动,感悟知识的发生、发展过程。
【自主学习 班级交流】



写出下列物质间转化的化学方程式。指出其中的化合反应和分解反应。
CO C CO2 CaCO3
=
1 \* GB3
①

= 2 \* GB3
②
= 3 \* GB3
③
H2CO3
= 4 \* GB3
④
。
|
知识点 |
学生活动 |
教师指导 |
|
(一)
CO2的物理性质 |
通常状态下,CO2是一种
、
的
,
密度比空气
,
溶于水,1体积水
的CO2,增大压强其溶解度
。固态CO2叫
,可
。
【实验1】向有高低不等的两支燃着蜡烛的烧杯里“倾倒”CO2气体,观察。
现象:
【实验2】向装满CO2气体的饮料瓶中倒入约 体积的水,盖好瓶盖,振荡,观察。 体积的水,盖好瓶盖,振荡,观察。
现象:
|
温馨提示:1、物理性质:一般要说明
、
、
、
、
等五点。
2、物质溶解情况分易溶、能溶(可溶)、微溶、难溶等层次,溶解情况一定要说准确。
3、【实验1】注意倾倒方式
【实验2】塑料瓶中的气体要收集满。 |
|
(二)
CO2的化学性质 |
1.CO2不支持可燃物的燃烧,本身也不燃烧。

(回忆实验1烧杯中蜡烛燃烧情况)
(例外:2Mg+CO2=======2MgO+C)
2.CO2与水反应形成碳酸(H2CO3)
【实验3】①两只试管中盛有紫色石蕊试液,分别向其中滴加稀HCl、醋酸,观察现象。
②向盛有紫色石蕊试液的试管中通入CO2气体观察;试管中液体变色后给该试管加热,观察实验现象:①
②
仔细阅读课本P118【实验6-5】,认真讨论,分析填写:
Ⅰ:干燥的CO2气体
使
变红。
Ⅱ:潮湿的CO2气体
使
变红,因为
|
思维点击:
1.CO2的灭火性不是万能的,镁带厂着火就不能用CO2灭火。不燃烧也不支持燃烧还有什么气体?
2.①注意H2CO3读作
,而不是
。碳酸不稳定,浓度稍大或稍加热,立即分解为
和
。
②【实验3】中做①、②实验是为了进行
。稀HCl和醋酸都呈酸性,可使紫色石蕊变
,说明
这种物质也具有
性。
回忆以前的内容:碱性物质可使
变
(如氨水) |
|
|
3、CO2与澄清的石灰水反应
【实验4】:将CO2气体通入澄清的石灰水中,观察现象:
化学反应方程式:
, |
该反应可检验CO2的存在。
|
【合作探究】
实验3①两只试管中盛有紫色石蕊试液,分别向其中滴加稀HCl、醋酸,观察现象。
②向盛有紫色石蕊试液的试管中通入CO2气体观察;试管中液体变色后给该试管加热,观察。
是什么使石蕊试液由紫色变红呢?是二氧化碳,还是水?或者它们在一起发生反应有新物质生成?
【教师点击】石灰浆抹墙壁,为加速墙壁硬化,常在室内放一个炭火盒,其原理:石灰浆的主要成分是氢氧化钙,炭火盆中的木炭燃烧时生成二氧化碳,二氧化碳与氢氧化钙反应,生成碳酸钙,碳酸钙是难溶于水的固体,墙壁就变坚硬了。由于在室内放了炭火盆,可以使二氧化碳的量增多,从而加快了石灰浆变成碳酸钙的速率,所以可以加速墙壁硬化。
【课堂检测】
基础达标
1、某气体完全燃烧,产物中含有二氧化碳,则该气体中(
)
A.一定含有碳元素
B.一定含有氧元素
C.一定含有碳氧两种元素
D.可能含有碳元素
 2、某同学设计了如下一组实验,取四朵用石蕊试液染成紫色的干燥纸花,分别按照下图进行实验。回答下列问题:
2、某同学设计了如下一组实验,取四朵用石蕊试液染成紫色的干燥纸花,分别按照下图进行实验。回答下列问题:
Ⅰ Ⅱ
Ⅲ
Ⅳ
(1)观察到纸花的颜色变化是:Ⅰ纸花变红;Ⅱ
;Ⅲ纸花不变色;Ⅳ
。(2)该同学进行的Ⅰ、Ⅱ两项实验,说明什么?(3)该同学进行四组对比实验的目的是什么?(用文字叙述)
(4)写出实验Ⅳ中发生反应的化学方程式:
。
综合运用
3.“千锤万凿出深山,烈火焚烧若等闲,粉身碎骨浑不怕,要留清白在人间。”每句包含什么变化,是化学变化的写出化学反应方程式。
拓展延伸
4.向澄清的石灰水中通入CO2气体,澄清的石灰水由澄清变浑浊,继续通CO2气体发现又有浑浊变澄清。滴水穿石就包含这个反应的原理:降落的雨水中溶有CO2,滴在石头上与石头中的CaCO3发生化学反应生成可溶物Ca(HCO3)2,慢慢将石头溶解。CaCO3+
CO2+H2O == Ca(HCO3)2(碳酸氢钙,易溶),加热后发现澄清液又变浑浊,化学反应方程式:Ca(HCO3)2===
CaCO3↓+CO2↑+H2O
自我评价:(突出学习方法及本节课主要内
签名:
年
月
日
同伴评价:(突出学习态度、过程表现与学习效果)
签名:
年
月
《课题3
二氧化碳和一氧化碳(第2课时)》学案
主备:李钢
审核:化学备课组
课型: 预习展示
【学习目标】
1. 了解CO2对生活和环境的影响,关注温室效应
2. 分析CO和CO2分子结构不同,了解CO和CO2在性质上的差异
3.
记住一氧化碳的可燃性、还原性和毒性
4.
记住一氧化碳的物理性质,一氧化碳的及其对环境的污染,加强环境保护意识。
【学法指津】通过学生预习、小组讨论、知识对比、教师指导来学习
【自主学习 班级交流】
知识回顾
|
知识点 |
学生活动 |
教师指导 |
|
(一)
CO2对生活和环境的影响 |
阅读课本P119-121内容
1、自然界产生CO2的途径:
2、自然界吸收CO2的途径:
3、温室效应①产生:大气中CO2含量不断上升;
可造成温室效应的气体有
、
、
、
等
②危害:A.
,B.
③防治措施:A.
B. ,C.
。 |
思维点击:
应当全面评价二氧化碳的功与过 |
|
(二)
CO2的用途 |
1.灭火,
2.气体肥料,促进植物光合作用
3.干冰作制冷剂、人工降雨;4.制汽水;
5.化工原料:制纯碱、尿素等 |
物质的
决定其用途。你能说出CO2的用途分别由什么性质决定的吗? |
|
(三)
CO的物理性质 |
在
下,CO是一种
、
的
。
溶于水,ρCO
;思考:收集CO的方法
,原因:
。 |
|
|
(四)
CO的化学性质 |

1.毒性:
;

2.
:2CO+ O2
====2CO2 火焰呈蓝色

3.
:CO+ CuO ==== Cu+
CO2
 3CO+
Fe2O3==== 2Fe+
3CO2 3CO+
Fe2O3==== 2Fe+
3CO2

|
1.煤炉里煤层上方的蓝色火焰,就是CO在燃烧。
2.仔细观察左图,最右边为什么用酒精灯去点燃尖嘴管?
|
|
(五)
CO的用途 |
1.作燃料
2.冶金工业上冶炼金属 |
分别对应CO的什么性质? |
|
本堂课小结 |
|
| |
|
|
|
【合作探究】1.CO2、CO都可致人死亡,(原理上)本质上有什么不同?
2. 如何除去
CO中混有少量CO2?
3. 如何除去CO2中混有少量CO?
 【教师点击】CO和CO2在分子结构上仅相差一个氧原子,但它们的性质却有很大的差异,这再一次说明,物质的结构决定其性质
【教师点击】CO和CO2在分子结构上仅相差一个氧原子,但它们的性质却有很大的差异,这再一次说明,物质的结构决定其性质
【课堂检测】
基础达标
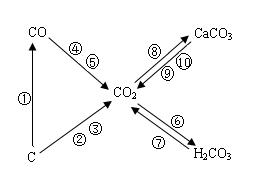
1.写出右图中的所有化学方程式:
= 1 \* GB3
①
,
= 2 \* GB3
②
,
= 3 \* GB3
③
,
= 4 \* GB3
④
= 5 \* GB3
⑤
,
= 6 \* GB3
⑥
,
= 7 \* GB3
⑦
,
= 8 \* GB3
⑧
,
= 9 \* GB3
⑨
,
= 10 \* GB3
⑩
。
2.区别CO和CO2的方法很多,下列方法不能用来区别的是
( )
A.分别通入紫色石蕊试液中,
B.分别通过灼热的CuO,
C.分别通入澄清的石灰水中,
D.用鼻子闻。
3.下列物质中,既有可燃性,又有还原性的化合物是
( )
A.CO2
B.CO
C.H2
D.C
4.在实验室里用CO还原氧化铜制取铜。若制取3.2g铜,需要氧化铜的质量是多少?
综合运用
5、将CO通入盛有Cu和CuO粉末共10g的试管中,加热使黑色粉末全部转变成红色后冷却,称得试管中Cu粉的质量为9g,求原混合物中CuO的质量分数。
拓展延伸
把CO2和CO的混合气体共20g通过足量的灼热的CuO中,完全反应后的气体质量变为28g,则原混合气体中CO2的质量是多少克?
自我评价:(突出学习方法及本节课主要内
签名:
年
月
日
同伴评价:(突出学习态度、过程表现与学习效果)
签名:
年
月